
GMP作为制药、食品等行业生产质量管理规范的强制性标准,无论是原料药、制剂、生物制品还是制药等企业都要掌握其要求,并按照GMP的规定去做。
硬件建设如厂房、设施等的改造或建设是药品生产企业实施GMP管理的基础,因此,要做出符合GMP要求的车间设计,并清楚明白怎样能设计出来,这是企业需要学习的。
制药企业设计GMP车间时遇到的问题
1、达不到GMP要求
1)设计单位对企业生产工艺和GMP要求不理解,生产企业对设计过程不了解,设计方案好像满足了GMP的要求,却在实际生产过程发生矛盾。
2)设计方案以原车间模式为样本,进行套用修改,不能与企业实际情况相结合,不能达到GMP要求,使企业GMP改造或建设留下硬伤。
2、建设成本高
3、操作麻烦,流程步骤多
如何能设计出符合GMP要求的车间?
合理的设计就是要使其在节约资金的同时,也能够符合GMP要求,保证药品质量。接下来,以一具体厂家为例,来探讨固体制剂综合车间的GMP设计。
1、了解企业生产要求和需求
该企业车间为固体制剂综合车间,主要生产片剂、胶囊和颗粒三种剂型的产品,且三种剂型为不同成分的产品。
由于全为固体制剂,该企业希望可以通过合并相同工段等方式,降低建设成本。
2、固体制剂综合车间的特征分析
(1)前段工序相同
该车间主要生产片剂、胶囊和颗粒三种剂型的产品,均为固体剂型,生产使用量大。
根据我国98版GMP,该三种剂型所要求的生产洁净级别相同,都是30万级;其前段制颗粒工序相同,如混合、制粒、干燥和整粒等,可集中共用;后段工序压片、包衣、胶囊填充不同,需分块布置;最后包装工序也有部分相同,也可集中设置。
因此,可以在同一车间生产这三种剂型,将生产线布置在同一洁净区内,这样可提高设备使用率,减少洁净区面积,从而节约建设资金。
(2)涉及物料种类多
由该车间主要生产片剂、胶囊和颗粒三种剂型的产品,且三种剂型为不同成分的产品,可知,该车间涉及物料种类多,可以设置物料暂存和中转站,明确人物流分离,加强人员的管理等措施来避免物料混淆。
(3)产尘的工序多
固体制剂生产过程中易产生大量的灰尘,该车间产尘工序多,在发尘量大的粉碎、过筛、制粒、干燥、整粒、总混、压片、充填等工段都需设计捕尘、除尘装置。并且应该把粉尘飞扬的的前工序区域联立在一起,组成前工序区域,从而有利于粉尘处理,保证药品质量。
(4)小批量、多品种
该车间生产片剂、胶囊剂、颗粒剂等多种剂型,生产的品种多,其各剂型的生产空间减小,产量低,适合小批量,多品种的产品生产,但不能同时生产多品种,所以应该在前段相同工序分设大小不同的设备隔间,供不同产量的产品生产,批与批之间必须严格清场,重视人员的管理,保证药品质量。
3、固体制剂综合车间的设计思路分析
固体综合制剂车间设计的法规依据是98版《药品生产质量管理规范》及其附录、《医药工业洁净厂房设计规范》(GB50457-2008)和国家关于建筑、消防、环保、能源等方面的规范。
参考设计规范标准
GMP要求车间的平面布局遵循以下特点:平面布局合理、严格划分区域、防止交叉污染、方便操作生产。
(1)人流物流设计
从目前国内制药装备水平来看,固体制剂生产还不可能全部达到全封闭、全机械化、全管道化输送,大量运送离不开人的搬运,人与人、物与物之间仍会发生交叉污染。
因此,需分别设置操作人员和物料出入口通道,最好设置相反方向(如:生产厂房的东面安排人流人口,西面安排物流人口);当设置同方向时,二者之间应保持相对较远距离,不得相互影响和妨碍。
(2)物料净化系统设计
物料与载体自身附着尘埃粒子和微生物,物料运动过程会将尘埃带入空气。因此,洁净室应设立独立的物料净化用室,包含外包装清洁、脱外包、缓冲气闸(传递窗或缓冲间)等;对容易污染环境的物料和废弃物应设专用出口。
如果工艺流程上合理,原辅料和直接接触药品的内包材料可以使用一个入口,贮存间根据产量确定面积。
固体制剂车间的生产能力和原辅料包装体积都很大,物料净化程序建议使用货淋或缓冲间,门是双门联锁结构,空调送风。
非无菌药物料净化示意图
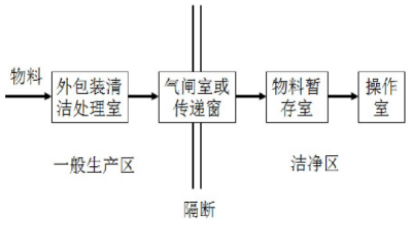
(3)人员净化设施设计
医药企业洁净车间的污染主要为微生物和尘埃粒子,而这些污染主要来源于人。因此,洁净室应设立独立的人员净化场所,包括雨具存放、换鞋、存外衣、盥洗、穿戴洁净工作服、气闸或空气吹淋室等,净化场所的洁净要求与生产区域相适应。
洁净室人员的一般净化程序
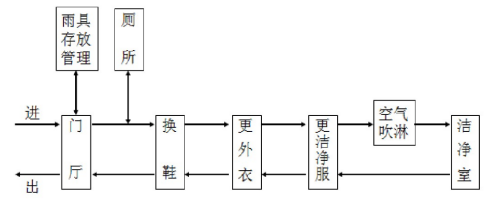
该车间只生产固体制剂,只有30万级的功能区和一般功能区两个等级的区域,所以可以分设两个人员更衣室,简化更衣的程序,减少污染。
另外,注意气闸室和风淋室门的数量及方向,经风淋时人数多需考虑是否设旁通门,经气闸室注意双门联锁。可以在气闸室内设置饮水机,方便员工饮水。
洁净衣的洗涤,我国GMP附录规定“10万级以上区域的洁净工作服应在洁净室(区)内涤、干燥、整理,必要时应按要求灭菌”。该厂为30万级的固体制剂厂,可以将洗衣房设在洁净区内,也可以设在非洁净区。洁净工作服的存放柜应采用不起尘、不腐蚀、易清洗、耐消毒的材料,如不锈钢、工程塑料等。
(4)生产设备布局设计
该车间为固体制剂综合车间,涉及物料量较大,应围绕中间站按工艺流程顺序布置各生产工序,要求各工序之间联系方便,快捷,上下工序相邻布置。生产区要有与生产规模相适应的面积和空间安排生产设备和物料,保证生产操作衔接合理,辅助设施应能在满足生产需要的同时,不妨碍生产操作。
固体制剂GMP综合车间设计(下),我们将重点讲解固体制剂相关工序的特殊要求,以及对比符合GMP车间设计的图纸和原设计图纸的不同,分析二者优缺点,直观地学习固体制剂GMP车间的设计。
推荐单位:中国药科大学
中国药科大学药品国内外注册与质量管理研究培训中心是一支专业能力强、年富力强,人员素质高,责任心强的团队,常驻企业一线,拥有丰富的实战经验。在仿制药一致性评价方面,中国药科大学仿制药一致性评价研究中心由4名教授、3名副教授、十余名从业近20年医务临床研究人员以及三十余名硕博士研究生组成。本团队还与中国科学院上海药物所、南京大学、南京医科大学、南京中医药大学、南京师范大学等兄弟院校相关研究团队密切合作。【详情点击(【震撼来袭】化工邦联合中国药科大学,为医药化工企业转型升级谋福利,大波重磅资源为邦友开启)】
注:上述内容由中国药科大学提供,想要了解更多,可联系化工邦。
浙ICP备16016599号